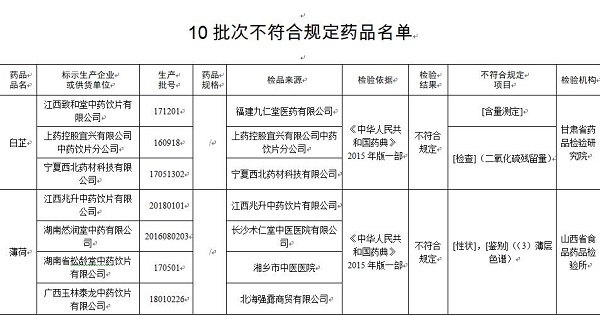
日前,國家藥監局官網發布通告稱,經甘肅省藥品檢驗研究院等4家藥品檢驗機構檢驗,標示為江西致和堂中藥飲片有限公司等10家企業生產的10批次藥品不符合規定。具體情況如下:
一、經甘肅省藥品檢驗研究院檢驗,標示為江西致和堂中藥飲片有限公司、上藥控股宜興有限公司中藥飲片分公司、寧夏西北藥材科技有限公司生產的3批次白芷不符合規定,不符合規定項目包括含量測定、二氧化硫殘留量。
經山西省食品藥品檢驗所檢驗,標示為江西兆升中藥飲片有限公司、湖南然潤堂中藥有限公司、湖南省松齡堂中藥飲片有限公司、廣西玉林泰龍中藥飲片有限公司、四川原上草中藥飲片有限公司生產的5批次薄荷不符合規定,不符合規定項目包括性狀、顯微特征、薄層色譜。
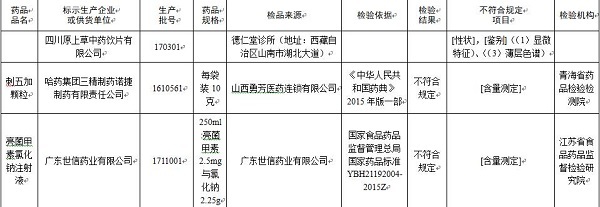
經青海省藥品檢驗檢測院檢驗,標示為哈藥集團三精制藥諾捷制藥有限責任公司生產的1批次刺五加顆粒不符合規定,不符合規定項目為含量測定。
經江蘇省食品藥品監督檢驗研究院檢驗,標示為廣東世信藥業有限公司生產的1批次亮菌甲素氯化鈉注射液不符合規定,不符合規定項目為含量測定。
二、對上述不符合規定藥品,相關藥品監督管理部門已采取查封、扣押等控制措施,要求企業暫停銷售使用、召回產品,并進行整改。
三、國家藥品監督管理局要求相關省級藥品監督管理部門對上述企業和單位依據《中華人民共和國藥品管理法》第七十三、七十四、七十五條等規定對生產銷售假劣藥品的違法行為進行立案調查,自收到檢驗報告書之日起3個月內完成對相關企業或單位的調查處理并公開處理結果。